Les produits biologiques sont exprimés à partir des hôtes de cellules bactériennes, de levures, d'animaux et de lignées cellulaires continues. Comme les produits biologiques sont produits à partir d'un substrat cellulaire, il est inévitable que l'ADN résiduel de la cellule hôte soit présent dans les produits finaux. Il présente des risques potentiels d'immunogénicité, d'oncogénicité et d'infectivité en raison de la tumeur ou des gènes liés au virus dans les lignées cellulaires de passage. L'ADN résiduel présente un risque potentiel élevé pour la sécurité et est considéré comme un attribut de qualité critique. Les agences actuelles, notamment l'OMS, l'UE et la FDA, ont limité les quantités acceptées d'ADN résiduel (moins de 10 ng ou 100 pg/dose). Parmi les méthodes de détection de l'ADN résiduel, la qPCR est considérée comme la plus pratique pour la quantification de l'ADN résiduel en raison de sa sensibilité, de sa précision, de sa précision et de son gain de temps.
Puisque l'ADNr peut provenir d'une grande variété d'hôtes, l'ADNr peut exister sous différentes tailles et formes physiques, différentes limites du contenu et de la taille de l'ADN peuvent être acceptables pour les organismes de réglementation si elles sont étayées par des preuves scientifiques et une évaluation des risques robuste. Le niveau de résidus d'ADN des cellules hôtes peut servir d'indicateur de la cohérence du produit et du contrôle de la qualité. La détection de l'ADN résiduel garantit la cohérence entre les lots de production et fournit une référence pour l'évaluation de la qualité du produit.
Pour analyser la concentration de l'ADN de la cellule hôte et la distribution de taille, les fractions d'ADN sont d'abord extraites de l'échantillon pour assurer la détection sans composés inhibiteurs de la matrice de l'échantillon. La séparation des billes magnétiques est la technologie la plus couramment utilisée à cette fin, permettant des processus d'extraction automatisés qui augmentent le débit et la précision.
Pour déterminer l'efficacité d'extraction de l'ADN résiduel des cellules hôtes, une quantité connue d'ADN cible (le «Spike») est ajoutée à l'échantillon avant l'extraction. En comparant la quantité d'ADN mesurée après extraction avec la quantité en pointe, l'efficacité d'extraction peut être calculée. Cette valeur d'efficacité est ensuite utilisée pour déterminer l'ADN résiduel de la cellule hôte dans l'échantillon. Une réduction de l'efficacité d'extraction indique la présence de composés inhibiteurs co-extraits avec l'acide nucléique.
Le développement d'une méthode de détection hautement sensible et spécifique pour l'ADN de cellule hôte en utilisant la PCR en temps réel nécessite une conception d'apprêt soigneuse et une optimisation de la réaction PCR. La spécificité et la sensibilité dePCR en temps réelSont influencés par la température de recuit, le temps et les concentrations de cations et d'amorces dans le tampon de réaction. Cibler un gène présent dans plusieurs copies peut augmenter la sensibilité du test.
La linéarité et la plage des méthodes de dosage ont été évaluées en calculant la droite de régression de la courbe standard. La précision a été évaluée en analysant le pourcentage de récupération des normes d'ADN à pointes à trois concentrations différentes. La précision intra-test et inter-dosage a été évaluée via le % CV de tous les QC à chaque niveau. La sensibilité a été déterminée en vérifiant le LOD et le LLOQ. La spécificité a été évaluée en analysant des échantillons d'ADN ou un pool d'ADN matriciel extrait de l'espèce/souche pertinente. La robustesse a été évaluée en évaluant la stabilité des performances du test dans différentes conditions de stockage.
La portée de validation du test d'ADN de cellule hôte résiduelle comprend:
Précision
Précision
Spécificité
Limite de quantification (LOQ)
Linéarité
Gamme
Robustesse
Un test entièrement validé permet l'utilisation de produits disponibles dans le commerce ou de kits spécialement conçus ciblant la séquence d'ADN hôte, ce qui le rend applicable aux tests parmi les produits biologiques.
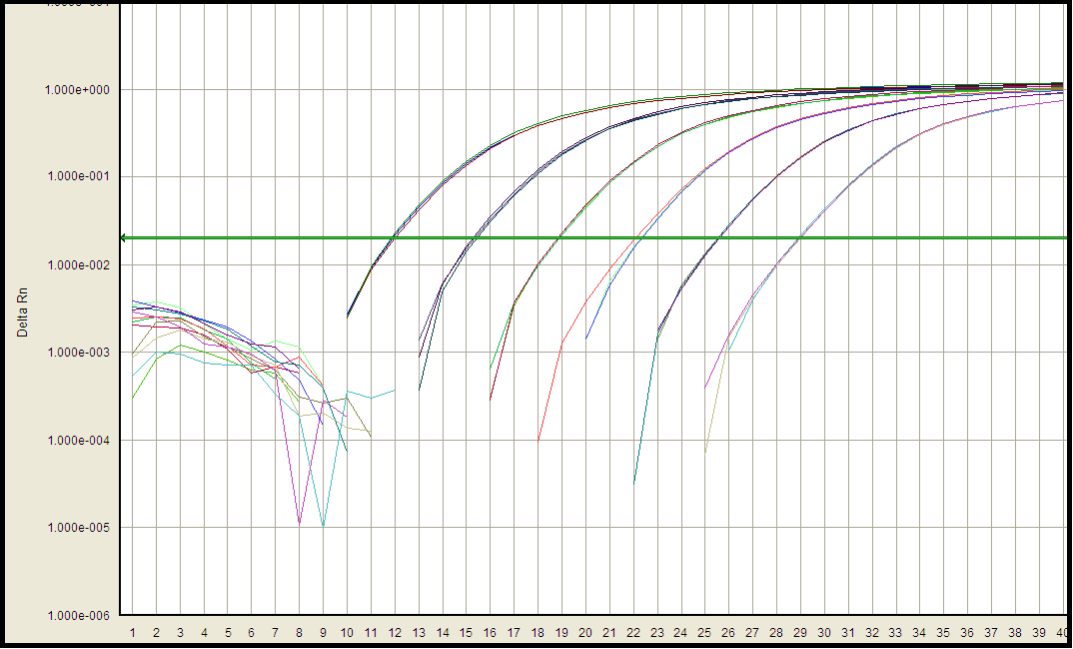
Étude de cas-Quantification de l'ADN de cellules hôtes résiduelles
CHO HCD Performance de validation-
Courbe standard: 96.6% d'efficacité d'amplification, coefficient de corrélation 0.999